
Après le variant Alpha (ex-variant B.1.1.7 dit britannique), le variant Beta (ex-variant B.1.351 dit sud-africain), le variant Gamma (ex-variant P.1 dit brésilien), le variant Delta (B.1.617.2 dit indien), c’est donc au tour d’un autre variant du SARS-CoV-2, dénommé Omicron (ou variant B.1.1.529), de faire les gros titres de la presse internationale et d’occuper le devant de la scène sur les chaînes d’info en continu. Ce nouveau variant est désigné GR/484A dans la base de données génomiques GISAID et correspond à la lignée (clade) 21K sur le site Nextstrain qui recense toutes les mutations du SARS-CoV-2 et analyse leur répartition géographique.
Le variant B.1.1.529 a été signalé pour la première fois à l’OMS en Afrique du Sud le 24 novembre. On rappelle que ce pays connait actuellement sa quatrième vague, les deux dernières ayant été causées par le variant Beta (initialement identifié en Afrique du Sud) et le variant Delta.
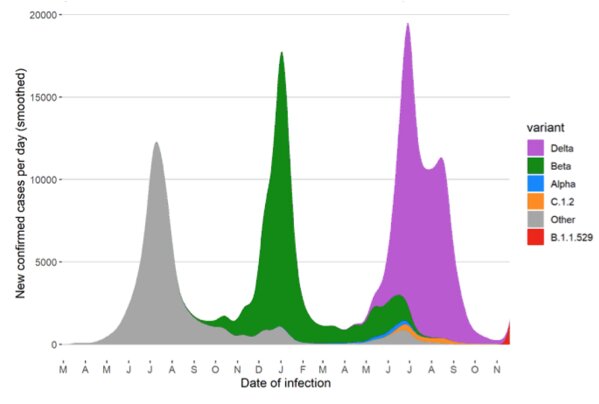
Or ces dernières semaines, alors que c’est l’été dans l’hémisphère sud, les infections ont connu une forte augmentation, coïncidant avec la détection du nouveau variant B.1.1.529. La première infection confirmée liée au variant B.1.1.529 provient d’un prélèvement réalisé le 9 novembre.
Ces derniers jours, la présence du variant Omicron a été détectée dans une dizaine de pays hors Afrique australe : Belgique, Hong Kong, Israël, Italie, Pays-Bas, Royaume-Uni, Allemagne, Danemark, République tchèque, Australie, Canada.
Les autorités de Hong Kong ont fait état de deux cas groupés chez des voyageurs. Des sources officielles israéliennes ont rapporté le cas d’un voyageur en provenance du Malawi et trois autres cas non associés à un voyage.
Le ministère belge de la santé a indiqué un cas chez un voyageur non vacciné. Des experts belges ont précisé le 26 novembre que la patiente infectée par B.1.1.529 est une jeune femme adulte qui a développé des symptômes 11 jours après avoir voyagé en Égypte via la Turquie. Elle n’a pas signalé de lien avec l’Afrique du Sud, ni avec d’autres pays d’Afrique australe. Elle n’était pas vaccinée et n’avait pas déjà été infectée. La patiente avait une charge virale élevée au moment du diagnostic (Ct de 14,2). Elle a développé un syndrome pseudo-grippal et ne présente donc pas de signes de maladie grave.
Quant au Botswana, ce pays a indiqué dans un communiqué de presse l’existence de quatre cas liés au variant Omicron, précisant que ces personnes étaient toutes complètement vaccinées et avaient été détectées lors d’un dépistage effectué avant un voyage.
Détecté à la mi-novembre au Botswana et en Afrique du Sud
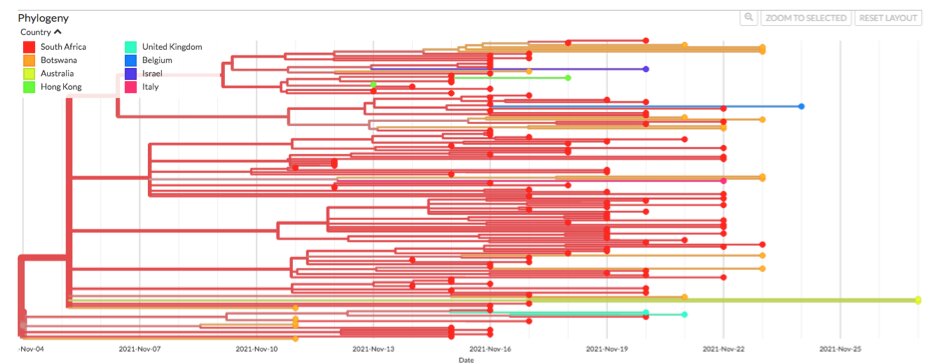
Ce nouveau variant a été détecté pour la première fois dans des prélèvements recueillis le 11 novembre 2021 au Botswana et le 14 novembre en Afrique du Sud. Il a été signalé dans la base GISAID le 23 novembre et a été désigné B.1.1.529 le 24 novembre. L’existence de ce variant B.1.1.529 a été communiquée à l’OMS le 24 novembre. Il a été baptisé VUI-21NOV-01 le 25 novembre.
Considéré le 24 novembre comme « variant sous surveillance » (VUM, Variants Under Monitoring), il a été étiqueté « variant préoccupant » (VOC, Variant of Concern) le 26 novembre par l’Organisation mondiale de la santé (OMS) et le Centre européen de contrôle et de prévention des maladies (ECDC).
Sur l’ensemble des échantillons biologiques recueillis en Afrique ces trente derniers jours, seuls le Botswana et l’Afrique du Sud ont rapporté des séquences génomiques du variant Omicron à un niveau correspondant à une transmission communautaire. Le 28 novembre, Botswana avait déposé 9 séquences, alors que l’Afrique du Sud en a quant à elle rapporté 109.
32 mutations, insertions et délétions dans la protéine spike
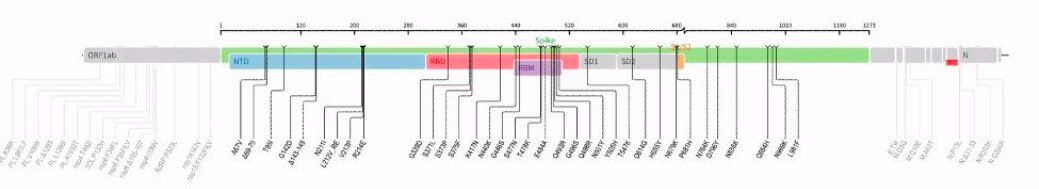
L’analyse des séquences a montré que par rapport au virus originel, ce nouveau variant renferme 30 mutations*, 3 petites délétions (pertes de matériel génétique) et une petite insertion, toutes situées dans le gène codant la protéine spike, protéine qui se lie au récepteur cellulaire ACE2 afin de permettre au virus de pénétrer dans les cellules qu’il infecte. Il y a un plus grand nombre de changements dans la protéine spike du variant B.1.1.529/Omicron que dans tout autre variant SARS-Cov-2 séquencé jusqu’à présent.
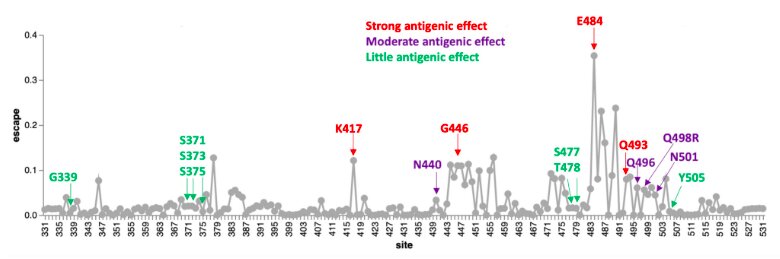
Parmi les mutations observées dans la protéine spike, celles situées en position 484 (E484A), 446 (G446S), 417 (K417N) et 493 (Q493R) retiennent particulièrement l’attention des chercheurs. En effet, il s’agit de mutations qui se situent dans des sites (épitopes majeurs) fortement impliqués dans l’échappement immunitaire (peak escape sites), autrement dit dans une diminution de la capacité de neutralisation des anticorps. En d’autres termes, on peut craindre que cela empêche la reconnaissance de la protéine spike par la grande majorité des anticorps produits, même lorsque ceux-ci sont dirigés contre plusieurs motifs différents de cette protéine (réponse polyclonale).
Ce nouveau variant comporte donc de multiples mutations sur la protéine spike, notamment dans le domaine de liaison au récepteur (RBD, receptor binding domain) et le site de clivage de la furine (mutations H655Y, N679K, P681H). On rappelle que le site de clivage de la furine joue un rôle majeur dans la fusion entre les membranes virale et cellulaire.
Plusieurs modifications présentes dans la séquence codant la protéine spike ont déjà été décrites dans les variants Beta et Delta. Elles sont associées à une transmissibilité accrue, à un échappement immunitaire ou à d’autres propriétés. De nombreuses mutations présentes dans le variant Omicron sont en revanche absentes dans d’autres variants préoccupants.
À ce propos, l’ECDC rappelle qu’un variant synthétique porteur de vingt mutations dans la protéine spike a été associé à un échappement immunitaire presque total vis-à-vis de sérums provenant de sujets Covid-19 convalescents et d’individus vaccinés. Cette étude, conduite par des chercheurs de l’université Rockefeller (New York), a été publiée le 20 septembre dans la revue Nature. Elle avait consisté à utiliser des pseudovirus, des virus porteurs d’une protéine spike hyper-mutée, en l’occurrence hébergeant vingt mutations naturellement observées dans des souches de SARS-CoV-2. Il avait été montré que ces virus artificiels étaient presque totalement résistants aux anticorps polyclonaux neutralisants produits chez des sujets convalescents ou chez des personnes ayant reçu un vaccin à ARN messager. Les chercheurs indiquaient cependant que le plasma d’individus auparavant infectés puis ultérieurement vaccinés avec un vaccin à ARN messager étaient parvenus à neutraliser ces pseudotypes porteurs d’une protéine spike polymutée.
Dans la mesure où Omicron porte encore plus de mutations dans le gène S par rapport au variant synthétique conçu par les chercheurs new-yorkais, « on peut s’attendre à un impact très significatif sur la capacité de neutralisation », estiment les experts de l’ECDC. En d’autres termes, le variant Omicron pourrait échapper de façon substantielle à l’action des anticorps neutralisants. En tout état de cause, soulignent-ils, « d’autres études virologiques et des études sur l’efficacité du vaccin sont nécessaires pour évaluer dans quelle mesure ce variant aura un impact sur l’efficacité du vaccin et sur la survenue d’infections post-vaccinales (breakthrough infections) ».
Une impressionnante constellation de mutations

Omicron est également caractérisé par la présence de 18 changements et délétions dans d’autres régions de son génome, en l’occurrence NSP3, NSP4, E, M et N, qui codent respectivement des protéines non structurales (NSP), la protéine d’enveloppe, la protéine de membrane et la nucléoprotéine. Il a récemment été montré que certaines mutations de la protéine N confèrent au virus une plus grande capacité à se répliquer et à se propager in vitro. Les virologistes parlent alors d’une augmentation de fitness du SARS-CoV-2 dans des cellules humaines.
Compte tenu du profil mutationnel d’Omicron, « un échappement immunitaire partiel est probable », estiment les experts de l’ECDC dans une note d’évaluation de la menace publiée en 26 novembre. Selon Penny Moore, virologue à l’université de Witwatersrand à Johannesburg, des données préliminaires font état de cas de réinfections et chez des personnes vaccinées, mais « à ce stade, il est trop tôt pour se prononcer ».
Le variant le plus divergent à ce jour
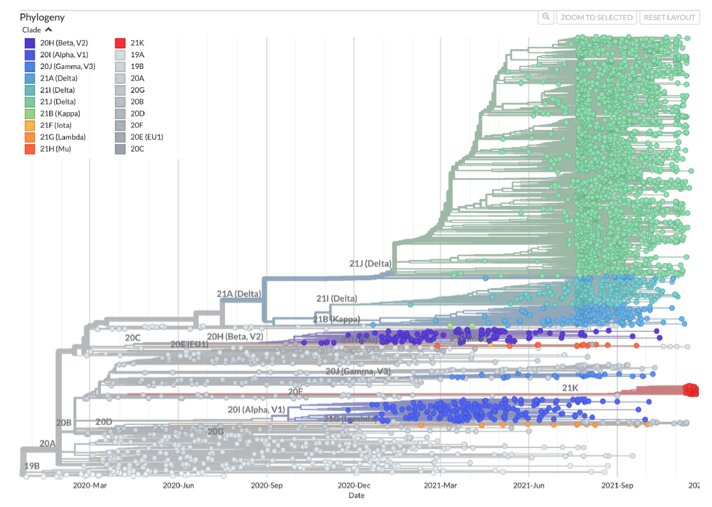
Les premières séquences génomiques disponibles provenaient de prélèvements réalisés au Botswana (6), en Afrique du Sud (58) et à Hong Kong (2). Les cinq premières séquences provenaient du Botswana, obtenues entre le 5 et 11 novembre.
Les données génomiques montrent que les cas du Botswana proviennent d’infections contractées en Afrique du Sud. Pour autant, insistent les experts belges, « cela ne signifie pas nécessairement que le variant Omicron a émergé en Afrique du Sud ». Une chose est sûre : l’Afrique du Sud est un des rares pays africains à disposer de capacités de séquençage génomique.
« Le variant Omicron est le variant le plus divergent ayant été détecté en quantités significatives jusqu’à présent au cours de la pandémie, ce qui soulève des inquiétudes quant au fait qu’il puisse être associé à une transmissibilité accrue, à une réduction significative de l’efficacité des vaccins et à un risque augmenté de réinfections », souligne l’ECDC. Et d’ajouter qu’il existe cependant « une incertitude considérable concernant la transmissibilité, l’efficacité vaccinale, le risque de réinfections ainsi que d’autres propriétés du variant Omicron ».
En conséquence, compte tenu d’un potentiel échappement immunitaire et d’une contagiosité potentiellement augmentée par rapport au variant Delta, les experts de l’ECDC déclarent que « la probabilité d’une nouvelle introduction et d’une propagation communautaire dans la région Europe est élevée ». Par ailleurs, dans une situation où le variant Delta ré-émerge actuellement dans la zone Europe, « l’impact de l’introduction et de la propagation éventuelle d’Omicron pourrait être très élevé », ajoutent-ils.
La menace représentée par le variant Omicron est prise au sérieux au Royaume-Uni. Selon le rapport technique de la UK Health Security Agency en date du 26 novembre, « d’après leur localisation dans le génome, la modélisation structurelle et l’expérience acquise avec d’autres variants, ces mutations pourraient modifier le comportement du virus en ce qui concerne l’échappement immunitaire, la transmissibilité et la sensibilité à certains traitements, en particulier les anticorps monoclonaux thérapeutiques ».
Résultats PCR discordants
Le génome du variant Omicron renferme également une délétion en position 69-70 dans la protéine spike, ce qui a comme conséquence une absence de détection du gène S (S gene target failure ou SGTF) aux tests PCR couramment utilisés (Thermo Fisher TaqPath). Ceux-ci reposent sur la détection de trois gènes cibles. Du fait de l’absence de détection du gène S, l’une des trois cibles n’est plus détectée, ce qui entraîne l’obtention de deux signaux au lieu de trois. Ces tests PCR dit discordants permettent ainsi, en première approximation, de détecter ce qui pourrait s’avérer être, après séquençage, un authentique variant Omicron.
Des enquêtes de surveillance ont été menées en Afrique du Sud en utilisant ces tests PCR discordants comme un moyen indirect de détection du variant Omicron. Elles ont montré une très forte augmentation d’incidence dans la plupart des provinces depuis la mi-novembre, l’augmentation la plus prononcée ayant été observée dans la province de Gauteng.
Une transmissibilité potentiellement plus élevée
En Afrique du Sud, environ 25 % de la population est complètement vaccinée. Le taux de vaccination complète chez les adultes est estimé à environ 37 % dans la province de Gauteng. Dans cette région la plus urbanisée du pays et qui comprend les villes de Pretoria et de Johannesburg, l’absence de détection du gène S (SGTF) a été observée dans plus de 50 % des prélèvements testés ces derniers jours. Le séquençage de 77 échantillons étiquetés SGTF provenant de Gauteng et collectés entre le 12 et le 20 novembre 2021, a confirmé qu’ils correspondaient tous au variant Omicron.
Cette transmissibilité potentiellement plus élevée du variant Omicron semble être confirmée sur l’analyse de données issues du séquençage et celles générées par les tests PCR. Des données, présentées lors d’une conférence de presse organisée par le ministre sud-africain de la santé le 25 novembre, indiquent que « le variant Omicron est déjà dominant dans le Gauteng et est présent en proportions significatives dans la plupart des régions d’Afrique du Sud. Globalement, le nombre de cas de Covid-19 augmente rapidement à Gauteng, bien que partant de faibles niveaux, et il est probable que cette augmentation soit due à la présence du variant Omicron », souligne l’ECDC. Selon le Pr Tulio de Oliveira (université Kwazulu-Natal), ce nouveau variant, retrouvé actuellement dans 75% des séquences génomiques analysées, représentera bientôt 100 % d’entre elles.
« Le rythme rapide de remplacement du variant Delta par Omicron en Afrique du Sud fait craindre que ce variant soit beaucoup plus transmissible que le Delta. Mais sachant que le nombre total de cas de Covid-19 en Afrique du Sud est actuellement faible [au 5 novembre, 258 cas détectés par jour], ceci pourrait proportionnellement amplifier l’effet de n’importe quels événements superpropagateurs impliquant un variant spécifique ». En d’autres termes, créer un effet loupe. Il importe donc de disposer de données supplémentaires pour estimer au mieux la capacité de transmission de ce nouveau variant, estiment les experts de l’ECDC.
Les experts belges ne disent pas autre chose. Le rapport du laboratoire national de référence, publié le 26 novembre sur le site de l’université de Louvain, précise que « l’évolution actuelle de ce variant est peut-être surestimée. Néanmoins, même si cet avantage d’un taux de croissance sans précédent (actuellement estimé à 38 % par jour) était plus faible, ce nouveau variant a très probablement encore un avantage de croissance suffisant pour devenir le variant dominant en Afrique du Sud et dans le reste du monde. En d’autres termes, ce variant pourrait avoir le potentiel de provoquer une nouvelle vague mondiale d’infections ».
L’OMS a publié, lundi 29 novembre, une note technique dans laquelle elle estime que « la probabilité qu’Omicron se répande au niveau mondial est élevée ».
Des enquêtes rétrospectives devraient également être réalisées à partir de prélèvements réalisés chez des voyageurs récemment venus de pays d’Afrique australe et détectés positifs pour le SARS-CoV-2, estiment les experts de l’ECDC.
Aucune information sur la capacité de réplication et la virulence
En tout état de cause, il importe d’analyser les données épidémiologiques à venir avec une grande attention, comme cela a été notamment réalisé après l’émergence en Inde du variant Delta. Il est également primordial d’étudier la capacité de réplication de ce nouveau variant en laboratoire dans des cellules humaines en culture.
On ne dispose à ce jour d’aucune information quant à savoir si une infection par Omicron se traduit par une maladie Covid-19 plus sévère que celle observée avec le variant Delta. Des données préliminaires en provenance d’Afrique du Sud indiquent qu’aucun symptôme inhabituel n’a été associé à Omicron et que certains individus infectés restent asymptomatiques, comme ce que l’on observe avec d’autres variants.
Importance plus que jamais cruciale des gestes et mesures barrières
Dans l’éventualité d’une baisse partielle ou totale de la protection conférée par les vaccins actuellement disponibles, l’ECDC insiste sur le fait que les mesures dites « non-pharmaceutiques » que représentent le port du masque, le contact tracing, la distanciation physique, l’aération correcte des espaces clos, restent encore efficaces pour contrôler la transmission. À cela s’ajoutent la mise en place du télétravail, la réduction de la foule dans les transports publics et l’hygiène des mains, souligne l’ECDC.
« Déjà nécessaires avant l’identification et émergence du variant Omicron, la mise en œuvre rapide, ou la réintroduction, des mesures non pharmaceutiques est essentielle, même dans les pays ayant un taux de vaccination élevée », souligne l’ECDC. Et d’ajouter qu’en raison du contexte épidémiologique actuel, combiné aux incertitudes liées à une évolution possiblement rapide de la situation concernant le variant Omicron, la mise en œuvre de l’ensemble de ces mesures doit intervenir de manière urgente dans la zone Europe.
Premiers résultats attendus dans deux à trois semaines
Des études sont actuellement entreprises par des équipes de recherche à travers le monde et les fabricants de vaccins pour déterminer la capacité neutralisante des sérums de patients convalescents et de sujets vaccinés vis-à-vis de pseudovirus mimant Omicron, à savoir des virus différents du SARS-CoV-2 (lentivirus) mais porteurs à leur surface d’une protéine spike comportant de nombreuses mutations présentes dans le nouveau variant.
D’autres travaux, menés dans des laboratoires de haute sécurité, seront également entrepris afin d’évaluer la capacité de ces mêmes sérums à neutraliser des isolats de virus vivants. « Ces données devraient être disponibles dans un délai de deux à trois semaines », indique l’ECDC.
Enfin, Moderna a indiqué son intention de développer une dose de rappel spécifique pour le nouveau variant Omicron. De son côté, le laboratoire allemand BioNTech, associé à Pfizer, a déclaré étudier ce nouveau variant et dit pouvoir disposer dans un délai de deux semaines des premiers résultats d’études visant à déterminer si le variant Omicron est capable d’échapper à la protection vaccinale.
Aujourd’hui, il semble prématuré de dire qu’il sera nécessaire d’adapter les vaccins à ce nouveau variant. Si tel était le cas, il devrait s’écouler au minimum trois mois avant de pouvoir disposer de vaccins à ARN messager spécifiquement conçus en fonction du profil génomique du variant Omicron. Outre le temps de conception – certes raccourci par rapport aux vaccins conventionnels et qui ne pourrait être que de six semaines – il faudra également compter avec les délais incompressibles de fabrication à très grande échelle et de livraison à de nombreux pays à travers le monde.
Risque d’évolution virale accélérée chez les immunodéprimés
Ce nouveau variant hébergeant une constellation de mutations, dans et hors la protéine spike, a probablement émergé à la faveur d’une infection prolongée par le SARS-CoV-2 chez un individu immunodéprimé, possiblement infecté par le virus du sida (VIH).
Sur ce blog, j’ai relaté, en juin 2021, l’histoire d’une patiente sud-africaine de 36 ans, séropositive pour le VIH et dont les tests RT-PCR pour le SARS-CoV-2 s’étaient révélés positifs pendant 216 jours, soit plus de sept mois. Chez cette patiente fortement immunodéprimée, l’équipe d’Alex Sigal et de Tulio de Oliveira (université du KwaZulu-Natal) avait observé l’émergence d’un variant porteur d’une trentaine de mutations, dont E484, K417 et N501 présentes dans le variant Beta (sud-africain).
Les chercheurs sud-africains y voyaient la résultante d’une évolution intra-hôte accélérée, autrement dit, la conséquence d’une infection prolongée par le SARS-CoV-2, de changements significatifs de la population virale, avec apparition de multiples mutations situées à des positions clés (épitopes) au sein de la protéine spike.
Ce cas clinique, rapporté le 4 juin 2021 sur le site de prépublication medRxiv, illustre donc le fait que des variants préoccupants peuvent émerger chez une personne immunodéprimée, porteuse d’une infection prolongée par le SARS-CoV-2 du fait d’une infection à VIH résistante aux antirétroviraux.
Plusieurs études ont été publiées ces derniers mois décrivant l’évolution intra-hôte du SARS-CoV-2 chez des patients immunodéprimés.
Des chercheurs allemands de l’université de Fribourg ont ainsi rapporté, le 4 novembre 2021 dans la revue Nature Communications, le cas d’un homme de 58 ans atteint de polykystose rénale devant recevoir une greffe de rein. Il reçoit un cocktail de trois médicaments immunosuppresseurs.
Malgré de strictes mesures de prévention, ce patient est dépisté positif pour le SARS-CoV-2 peu de temps après le début de son traitement. Les prélèvements de l’écouvillonnage nasal ont été utilisés pour tenter d’isoler du virus dans des cellules en culture. Cela a été effectivement le cas, ce qui a confirmé l’excrétion de virus infectieux. Malgré l’allègement du traitement immunosuppresseur (arrêt du mycophénolate mofetil entre J123 et J141), le test PCR est toujours positif pour le SARS-CoV-2 plus de quatre mois et demi plus tard (J140).
Alors que le taux d’anticorps oscillait aux alentours du seuil de détection jusqu’alors, le patient commence à J140 à enfin développer des anticorps spécifiques du SARS-CoV-2. Le patient reçoit ensuite l’antiviral remdésivir pendant 10 jours. Le test PCR se négative finalement au bout du 189e jour. Le patient sera donc resté positif pour le SARS-CoV-2 pendant plus de six mois. Le virus ne sera plus par la suite isolé dans les cultures cellulaires, ce qui indique que l’infection a disparu.
Alors que le virus n’avait pas acquis de mutations durant les deux premières semaines, plusieurs sont apparues à partir du 42e jour. Certaines se sont accumulées au fil du temps. Les changements les plus notables ont été observés dans le gène S, tant au niveau du domaine RBD que du domaine NTD (domaine N-terminal, N-terminal domain), respectivement situés sur la pointe et sur le côté de la protéine spike. On rappelle que le RBM est la région de la protéine skipe entrant en contact direct avec le récepteur cellulaire ACE2 (qui sert de porte d’entrée au SARS-CoV-2 dans les cellules qu’il infecte). Il s’avère que les variants persistants présents chez ce patient immunodéprimé partagent des mutations avec celles observées chez les variants préoccupants détectés au Royaume-Uni, en Afrique du Sud et au Brésil.
À l’instar de l’étude sud-africaine consacrée à une patiente VIH+, cette étude allemande montre donc que chez les patients immunodéprimés ayant une infection à SARS-CoV-2 persistante, l’évolution du virus est accélérée par rapport à ce que l’on observe parmi les souches virales circulantes. Ces dernières n’acquièrent qu’un petit nombre de mutations au fil du temps, à un rythme relativement constant d’environ une à deux mutations par mois.
Infection virale persistante pendant 355 jours
Publié le 5 octobre 2021 sur medXriv, une étude menée par des chercheurs américains de l’Institut national des allergies et des maladies infectieuses (NIAID, Bethesda, Maryland) a rapporté le cas d’une patiente immunodéprimée présentant une infection persistante par le SARS-CoV-2 s’accompagnant de légers symptômes. Cette femme, âgée d’une quarantaine d’années, diabétique et souffrant d’un lymphome à cellules B, avait avait été traitée trois ans auparavant par plusieurs cycle d’immunothérapie cellulaire (cellules CAR-T) pour son lymphome, ce qui avait entraîné une immunosuppression durable du fait d’une déplétion en cellules B (baisse des lymphocytes B impliqués dans la production d’anticorps).
Le virus a accumulé une délétion particulière dans le domaine amino-terminal NTD de la protéine spike ainsi qu’une perte de matériel génétique dans deux régions de son génome (délétion complète de ORF7b et quasi-complète de ORF8). Une délétion d’une telle longueur (couvrant 497 nucléotides) n’avait encore jamais été décrite chez un patient immunodéprimé. Il s’agit de la plus longue délétion rapportée à ce jour dans le génome du SARS-CoV-2.
La patiente a alors été traitée par remdésivir et a reçu du plasma de patients Covid-19 convalescents, avec pour conséquence la disparition de l’infection au 355e jour. Il s’agit de la plus longue durée d’infection par le SARS-CoV-2 rapportée à ce jour.
Marc Gozlan (Suivez-moi sur Twitter, Facebook, LinkedIn)
* Le variant Omicron est caractérisé par les mutations suivantes dans la protéine spike : A67V, D614G, D796Y, E484A, G142D, G339D, G446S, G496S, H69del, V70del, H655Y, ins214EPE, K417N, L212I, L981F, N211del, N440K, N501Y, N679K, N764K, N856K, N969K, P681H, Q493R, Q498R, Q954H, S371L, S373P, S375F, S477N, T95I, T478K, T547K, V143del, Y144del, Y145del, Y505H. Ces mutations se situent dans le domaine RBD (receptor binding domain, région entrant en contact avec le récepteur cellulaire ACE2 qui sert de porte d’entrée au SARS-CoV-2 dans les cellules qu’il infecte) et dans le NTD (domaine N-terminal, N-terminal domain).
Pour en savoir plus :
Threat Assessment Brief. Implications of the emergence and spread of the SARS-CoV-2 B.1.1. 529 variant of concern (Omicron) for the EU/EEA 26 November 2021. (ECDC)
Genomic surveillance of SARS-CoV-2 in BelgiumReport of the National Reference Laboratory (UZ Leuven & KU Leuven). Situation update – 26 of November 2021 (report 2021_56)
Weigang S, Fuchs J, Zimmer G, et al. Within-host evolution of SARS-CoV-2 in an immunosuppressed COVID-19 patient as a source of immune escape variants. Nat Commun. 2021 Nov 4;12(1):6405. doi: 10.1038/s41467-021-26602-3
Nussenblatt V, Roder AE, Das S, et al. Year-long COVID-19 infection reveals within-host evolution of SARS-CoV-2 in a patient with B cell depletion. medRxiv [Preprint]. 2021 Oct 5:2021.10.02.21264267. doi: 10.1101/2021.10.02.21264267
Schmidt F, Weisblum Y, Rutkowska M, et al. High genetic barrier to SARS-CoV-2 polyclonal neutralizing antibody escape. Nature. 2021 Sep 20. doi: 10.1038/s41586-021-04005-0
Hensley MK, Bain WG, Jacobs J, et al. Intractable Coronavirus Disease 2019 (COVID-19) and Prolonged Severe Acute Respiratory Syndrome Coronavirus 2 (SARS-CoV-2) Replication in a Chimeric Antigen Receptor-Modified T-Cell Therapy Recipient: A Case Study. Clin Infect Dis. 2021 Aug 2;73(3):e815-e821. doi: 10.1093/cid/ciab072
Greaney AJ, Starr TN, Barnes C, et al. Mapping mutations to the SARS-CoV-2 RBD that escape binding by different classes of antibodies. Nat Commun. 2021 Jul 7;12(1):4196. doi: 10.1038/s41467-021-24435-8
Avanzato VA, Matson MJ, Seifert SN, et al. Case Study: Prolonged Infectious SARS-CoV-2 Shedding from an Asymptomatic Immunocompromised Individual with Cancer. Cell. 2020 Dec 23;183(7):1901-1912.e9. doi: 10.1016/j.cell.2020.10.049
Choi B, Choudhary MC, Regan J, et al. Persistence and Evolution of SARS-CoV-2 in an Immunocompromised Host. N Engl J Med. 2020 Dec 3;383(23):2291-2293. doi: 10.105
Sur le web :
Variant: 21K (Omicron). covariants.org




 World Opinion | Alternative Média زوايا ميادين | صوت من لا صوت له Débats De Société, Questions, Opinions et Tribunes.. La Voix Des Sans-Voix | Alternative Média
World Opinion | Alternative Média زوايا ميادين | صوت من لا صوت له Débats De Société, Questions, Opinions et Tribunes.. La Voix Des Sans-Voix | Alternative Média




